好氧/ 除磷顆粒對亞硝化顆粒污泥啟動




厭氧氨氧化工藝以其經濟、高效等優勢在國內外污水處理廠得到推廣應用.厭氧氨氧化工藝目前公認的化學計量式如式(1)所示.

有研究表明, 沉降性良好, 結構緊密的好氧顆粒污泥有助于實現亞硝化污泥顆粒化.通過接種大量的好氧顆粒污泥, 調整進水基質, 把處理高有機負荷的好氧顆粒轉變到處理高氨氮負荷的亞硝化顆粒污泥, 但是該研究中需要大量的好氧顆粒污泥作為接種污泥, 而好氧顆粒污泥的馴化時間較長.因此, 在亞硝化絮狀污泥系統中添加部分好氧顆粒污泥誘導亞硝化顆粒污泥的研究很有必要.Wu等、王然登等的研究表明, 在強化生物除磷系統的厭氧階段釋放磷時會有大量的帶正電的微粒生成, 這些微粒可作為顆粒污泥的晶核吸附帶負電的細胞體, 進而促進顆粒污泥的生成.因此, 在絮狀污泥中添加部分除磷顆粒誘導顆粒化的研究很有意義.'本文實驗在R1反應器中不添加顆粒污泥, 在R2、R3中分別添加20%好氧顆粒污泥、20%除磷顆粒污泥.通過比較3個反應器粒徑變化、MLSS、SVI、EPS等參數, 研究不同顆粒污泥對亞硝化顆粒污泥啟動的影響, 并比較了其亞硝化性能, 以期為快速啟動亞硝化顆粒污泥提供理論依據.
1 材料與方法 1.1 SBR反應器運行
實驗采用3組相同規格的SBR反應器, 均由有機玻璃制成, 高70 cm, 內徑15 cm, 有效容積是10.5 L, 換水比是2/3, 底部設有曝氣裝置, 采用鼓風曝氣, 轉子流量計控制曝氣量. 3組SBR反應器均在室溫(22~28℃)下進行. SBR反應器每天運行3個周期, 每個周期8 h, 其中包括12 min進水、厭氧攪拌202~218 min、4 h曝氣攪拌、沉降時間由20~4 min遞減, 3 min排水和3 min閑置.不同階段反應器運行參數見表 1.

1.2 實驗用水和接種污泥
3組SBR反應器均接種取自高碑店污水處理廠的絮狀污泥作為種泥.反應器接種污泥后MLSS為(2 700±200) mg·L-1、SVI為140 mL·g-1.采用人工配水模擬生活污水啟動反應器, 以丙酸鈉為有機碳源, 硫酸銨提供氨氮100~250 mg·L-1, 碳酸氫鈉調節進水堿度, 堿度與NH4+-N濃度質量比為10 :1, 每升水中含有0.136 g KH2PO4、0.02 g MgSO4·7H2O、0.136 g CaCl2, 同時還有微生物生長必需的微量元素.
實驗分為S1、S2、S3這3個階段:S1階段為亞硝化階段, 采用低碳氮比的人工配水啟動亞硝化; S2階段為亞硝化污泥顆粒化階段, 通過在R2、R3反應器中分別添加20%的好氧顆粒污泥、20%除磷顆粒污泥以期加快顆粒化進程; S3階段為強化顆粒化階段, 通過增加進水中的COD負荷和氨氮負荷, 促使亞硝化顆粒增大和提高系統的亞硝化性能.
1.3 分析方法
NH4+-N、NO2--N、NO3-N、SS、VSS、SVI等均采用國家規定的標準方法測定, 進水氮素的測定是在進水后2 min, 取樣經濾膜過濾后測定. pH、DO及溫度的測定采用WTW(Ph/Oxi 340i)便攜式多參數測定儀.污泥形態采用光學顯微鏡(Olympus BX51)進行觀察和記錄.污泥的粒徑分布采用激光粒度儀(Malvern Mastersizer 2000)進行測定.
本實驗中氨氧化率、亞硝化率, 游離氨(FA)和游離亞硝酸(FNA)分別按照式(2)~(5)計算式中, ρ(NO2--N)、ρ(NO3--N)是進出水中NO2--N、NO3--N的濃度差, mg·L-1; ρ(NH4+-Nin)為進水NH4+-N濃度, mg·L-1; ρ(NH4+-Ninner)、ρ(NO2--Ninner)是反應器內NH4+-N、NO2--N濃度, mg·L-1.
2 結果與討論 2.1 亞硝化快速啟動
運行期間, 反應器R1、R2、R3進出水氨氮濃度及亞硝化率如圖 1所示.從中可知, 由于接種污泥不能很好地抑制亞硝酸鹽氧化菌(NOB), 故反應器中亞硝化率為0.由于AOB的“飽食饑餓”特性, 從厭氧階段到好氧階段AOB較NOB更快地恢復, 所以厭氧/好氧的運行方式下, 以及通過高FA和FNA的聯合抑制下, 系統的亞硝化率逐漸升高.在第7個周期(3 d)時, 當進水氨氮濃度由50 mg·L-1提高到100 mg·L-1后, 由于硝化細菌抵抗氨氮負荷沖擊能力弱, 故出水氨氮濃度隨之升高.但隨著培養周期的延長, 硝化細菌抗氨氮負荷沖擊能力逐漸增強, 故出水氨氮濃度逐漸降低, 亞硝化率逐漸升高.基于以上原因, 在第19個周期(6 d)時, 當進水氨氮濃度由100 mg·L-1提高到200 mg·L-1后, 同樣出現了出水氨氮濃度先升高后降低的現象, 但亞硝化率一直保持上升的趨勢.由圖 1(a)可知, 當R1運行至第57個周期(19 d)時, 亞硝化率已高達92%, 并且仍有升高趨勢, 最高達到96%, 連續7個周期亞硝化率超過90%, 故亞硝化啟動成功.由圖 1(b)和圖 1(c)可知, 當R2和R3運行至57個周期(19 d)時, 亞硝化率分別高達93%和92%, 并且連續7個周期穩定在90%以上, 亞硝化啟動成功.
2.2 亞硝化顆粒污泥形成過程 2.2.1 污泥顆粒物理性質變化
R1、R2、R3啟動初期接種的普通活性污泥為黑色絮狀體, 歷經57個周期(19 d)的馴化培養后, 污泥顏色呈現淺黃色. R1在第30 d時, 出現白色的細小顆粒且在其周圍富集絮狀污泥.如圖 2所示, R1在第76 d時, 反應器內顆粒的平均粒徑達到412 μm, 成功實現顆粒化, 這可能是由于微生物在一定條件下會發生自凝聚且微生物有附著生長傾向的原因.在S3階段(57~108 d), R1中顆粒粒徑增加的速率明顯高于S2階段, 這主要因為增加COD負荷刺激異養細菌產生更多利于硝化細菌黏附和聚集生長的EPS, 促進亞硝化顆粒的增大.在運行末期(108 d), R1顆粒平均粒徑達到689 μm, 其中71.54%的顆粒在500 μm以上.
在第23 d, 分別向R2、R3反應器接種20%好氧顆粒污泥和20%除磷顆粒污泥, R1不接種顆粒污泥.實驗中添加的好氧顆粒污泥是取自人工配水的SBR反應器, 反應器進水中COD濃度為300 mg·L-1、NH4+-N濃度為30 mg·L-1、KH2PO4-P濃度為5 mg·L-1, C、N、P的去除率達到95%、83%、90%, MLSS為4200 mg·L-1, SVI為34 mL·g-1; 添加的除磷顆粒是取自人工配水的SBR反應器, 反應器進水中KH2PO4-P濃度為10 mg·L-1, P的去除率達到95%, MLSS為4280 mg·L-1, SVI為32 mL·g-1.
如圖 2所示, 在第26 d, R2平均粒徑由初始182 μm下降到150 μm, 接種的好氧顆粒污泥發生裂解, 其原因可能是:①由于低C/N比的進水基質, 導致顆粒中的異養細菌大量死亡; ②接種后大量絮狀污泥附著在好氧顆粒污泥表面, 堵塞了好氧顆粒輸送基質的通道, 導致顆粒內部的微生物發生自溶.在第27 d, 基于同樣的原因, 接種的除磷顆粒污泥發生了裂解, R3平均粒徑由196 μm下降到160 μm.且R2中顆粒粒徑大于800 μm的顆粒百分比由18%下降到5%, 由于接種的除磷顆粒能很好地適應厭氧/好氧的運行方式只有小部分大顆粒發生了裂解, 故R3中顆粒粒徑大于800 μm的顆粒百分比由20%僅下降到12%.
分析圖 2可知, 在第42 d時, 由于小顆粒表面能的作用和自身多孔介質, 故會吸附絮狀污泥, R2反應器中顆粒平均粒徑達到468 μm, 成功實現顆粒化并且比R1顆粒化時間少34 d, 說明在反應器中添加好氧顆粒污泥顆粒可以加快亞硝化顆粒污泥的形成.在S3階段(57~108 d), R2中顆粒同樣快速增大, 在運行末期(108 d), R2中顆粒平均粒徑達到893 μm, 其中72%的顆粒粒徑達到600 μm以上, 說明添加好氧顆粒后啟動的亞硝化顆粒污泥系統更有利于大粒徑顆粒的形成.基于以上原因, 在第56 d時, R3中顆粒粒徑達到400 μm, 同樣成功實現了亞硝化污泥顆粒化, 且比R1成功實現顆粒化提前20 d, 但與R2實現顆粒化時間相差不大.但在S3(57~108 d)階段, R3發生了污泥膨脹(機制在2.2.2節進行說明), 由于大量的絲狀菌附著在亞硝化顆粒表面, 顆粒發生裂解, 顆粒粒徑在運行末期(108 d)下降到200 μm, 且仍有下降趨勢.說明高COD負荷[0.5 kg·(m3·d)-1]和高氨氮負荷[0.5 kg·(m3·d)-1]容易破壞添加除磷顆粒誘導形成的亞硝化顆粒污泥系統.
2.2.2 運行階段MLSS和SVI的變化
如圖 3所示, 在S1階段(0~22 d), R1、R2、R3的污泥濃度MLSS分別由2 770、2 541、2 760 mg·L-1降至2 493、2 732、2 469 mg·L-1. 3組反應器的MLSS均呈現下降趨勢.這可能是因為: ①低C/N的進水, 抑制了異養細菌的生長; ②反應周期中厭氧階段, 限制了細菌生長; ③NO2--N具有一定的毒性, 抑制細菌生長.由于3組反應器在運行中一些沉降性較差的絮狀污泥不斷流失, 故3組反應器SVI值均減小, 活性污泥的沉降性變好.
在S2階段(23~56 d), 沉降時間由20 min降低至4 min, 形成較大的選擇壓加快顆粒形成.在第23 d, 分別向R2、R3反應器中接種20%的好氧顆粒污泥和20%的除磷顆粒污泥, R1不接種誘導顆粒污泥.分析圖 3(a)可知, R1由于沉降時間的減少, 大量的絮狀污泥流失, MLSS出現急劇的下降.在第56 d, R1中MLSS降至647 mg·L-1.分析圖 3(b)和3(c)可知, 由于絮狀污泥黏附在顆粒污泥表面形成良好的污泥持留, 故R2、R3中MLSS沒有出現大的下降.在第56 d, R2、R3中MLSS分別為2 591 mg·L-1、2 562 mg·L-1.
在S3階段(57~108 d), 如圖 3(a)和3(b)所示, 當進水中的氨氮負荷由0.4 kg·(m3·d)-1增加到0.5 kg·(m3·d)-1, COD負荷由0.2 kg·(m3·d)-1增加到了0.5 kg·(m3·d)-1后, R1、R2由于C/N比的增加, 導致異養細菌(反硝化細菌)快速增殖, 進而致使MLSS增加.在運行末期(108 d), R1反應器MLSS穩定在2415 mg·L-1, R2反應器MLSS穩定在3012 mg·L-1.由于較低的沉降時間致使沉降性差的絮狀污泥流失, 因此R1、R2的SVI值均呈現下降的趨勢, 沉降性能變好.在運行末期(108 d), R1、R2的SVI值分別為62 mL·g-1、42 mL·g-1.
分析圖 3(c)可知, 在運行末期(108 d), R3中MLSS為2 000 mg·L-1, 且呈現下降趨勢; SVI值為134 mL·g-1, 且呈上升趨勢.說明高COD負荷[0.5 kg·(m3·d)-1]和高氨氮負荷[0.5 kg·(m3·d)-1]容易破壞添加除磷顆粒形成的亞硝化系統的沉降性能, 及造成系統污泥大量流失. R3發生污泥膨脹可能的原因是:①由于增加了進水COD負荷, 導致添加的除磷顆粒中聚糖菌和絲狀細菌成為優勢菌, 導致污泥膨脹; ②氨氮和亞硝酸鹽對于除磷顆粒系統有很大的影響, 加入不同濃度的亞硝酸鹽氮和氨氮后均發生了污泥膨脹.但是由于接種的好氧顆粒污泥中有豐富的微生物相, 故誘導形成的亞硝化顆粒污泥系統能抵御環境的變化, 耐沖擊負荷, 更快適應水質變化.
2.2.3 運行階段胞外聚合物EPS的變化
如圖 4所示, 在S1階段(0~22 d)進水氨氮濃度從50 mg·L-1增加到200 mg·L-1后, 由于高的氨氮濃度會抑制細胞活性, 致使細胞分泌的PN量減少, 故R1、R2、R3三組反應器的EPS量無增加趨勢, 且PN/PS呈現出下降趨勢.在S2階段(23~56 d), 反應器中的微生物為了適應沉降時間縮短形成的選擇壓, 微生物釋放的EPS急劇增加, R1、R2、R3中EPS量分別由78.1、81.4、81.4 mg·g-1增加到142.8、176.4、164 mg·g-1.如圖 4(a)所示, 在第23 d, R1中PN/PS為1.2, 且呈上升趨勢, 由于細胞表面的疏水性主要是含更多疏水鍵的PN含量決定的, PN/PS值的升高會促使污泥顆粒形成, 第56 d時, PN/PS為2.4.如圖 4(b)和4(c)所示, R2、R3相比于R1的PN/PS值增長速率較大, 在第23 d、56 d分別為1.2和1.19、3.2和2.7.說明添加顆粒的R2和R3中污泥表面有更強的疏水性, 污泥顆粒化更容易形成.
在S3階段(57~108 d), 由于進水中COD負荷的提升, 異養微生物可利用基質增多, 增殖速率升高, 微生物數量逐漸增多, 微生物分泌的EPS量較高.分析圖 4(a)和4(b)可知, 在S3階段, R1和R2中EPS量增加.隨著運行時間的延長, 系統中的微生物逐漸適應環境, 微生物分泌的EPS逐漸趨于穩定.在運行末期R1、R2中EPS分別穩定在159 mg·g-1、164.6 mg·g-1.分析圖 4(c)可知, R3中由于膨脹污泥會消耗大量的營養物質, 故EPS中多糖和蛋白質均呈現出了下降, 但多糖的含量發生較大的下降致使PN/PS的變化呈現上升的趨勢.
2.2.4 運行階段氮素的變化
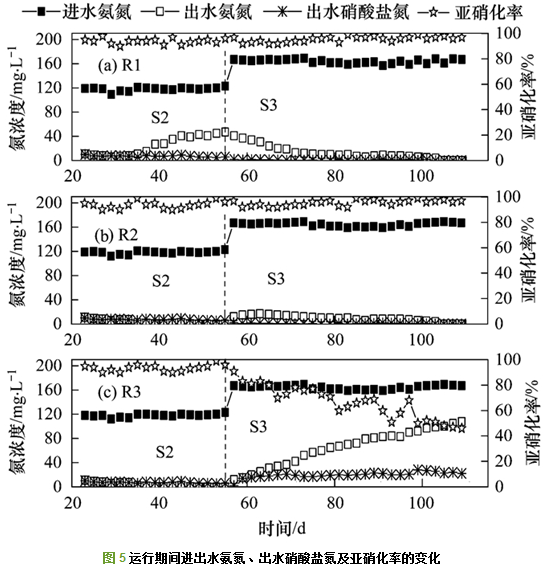
如圖 5(a)所示, 在S2階段(23~56 d), 由于沉降時間的縮短, 大量的絮狀污泥流失, R1中的AOB數量減少, 故出水氨氮濃度呈現上升的趨勢.隨著運行時間的延長, R1中AOB數量逐漸增加, 故出水中氨氮濃度呈現下降趨勢.在運行末期(108 d), 出水氨氮濃度達到0 mg·L-1.運行期間, R1出水硝酸鹽氮一直保持很低的水平, 運行末期(108 d), 出水硝酸鹽濃度為0 mg·L-1, 說明R1中NOB得到很好地抑制.有研究表明, 游離氨(FA)濃度在6~9 mg·L-1時, NOB就會停止生長; 游離亞硝酸(FNA)濃度在0.023 mg·L-1時就會完全抑制NOB, 在0.4 mg·L-1時就會完全抑制AOB.本實驗中FA的變化范圍是0.48~21.09 mg·L-1, FNA的變化范圍是0.000 7~0.023 mg·L-1, 故在此FA和FNA的變化范圍內會完全抑制NOB生長, 故R1在運行期間保持很好的亞硝化性能, 亞硝化率保持90%以上.
如圖 5(b)所示, 相比于R1, R2中AOB數量穩定故出水氨氮很低, 在運行末期(108 d)出水氨氮為0 mg·L-1, 出水硝酸鹽氮為0 mg·L-1, 且亞硝化率一直保持在90%以上.說明在厭氧/好氧的間歇曝氣方式、FA和FNA的聯合控制下, NOB得到了很好地抑制, R1和R2保持良好的亞硝化性能.如圖 5(c)所示, R3在S2階段有良好的亞硝化性能, 出水氨氮保持很低.在S3階段, 由于R3中發生了污泥膨脹, 故MLSS急劇下降, AOB的濃度也減少, 因此出水的氨氮上升.由于大量增加的異養細菌(絲狀菌)會與硝化細菌爭奪有限的空間和溶解氧, 導致系統硝化性能變差, 亞硝化率出現下降趨勢, 由91%下降到運行末期(108 d)的46%, 同時系統中游離亞硝酸鹽的量較S2階段少, 不足以抑制NOB, 導致出水硝酸鹽增加.
2.2.5 周期內COD、亞硝酸鹽氮、硝酸鹽氮變化
R1、R2穩定運行階段中, COD、氨氮、亞硝酸鹽氮及硝酸鹽氮的變化, 如圖 6(a)所示, 在厭氧階段, R1由于缺乏溶解氧, 故反應器中氨氮濃度由154 mg·L-1僅降低到146 mg·L-1, 但在曝氣階段氨氮濃度迅速下降, 氨氮容積去除負荷平均達到0.42 kg·(m3·d)-1與蘇東霞等在曝停比3:3時, 所得的氨氮容積去除負荷0.4 kg·(m3·d)-1接近; 如圖 6(b)所示, 在厭氧階段, R2中的氨氮濃度由156 mg·L-1僅降低到150 mg·L-1, 在曝氣階段氨氮濃度迅速下降, 氨氮容積去除負荷達到0.426 kg·(m3·d)-1.本研究中, 進水總氮就是進水氨氮和上一周期剩余在反應器中亞硝酸鹽氮及硝酸鹽氮之和, 出水總氮是反應剩余的氨氮和反應生成的亞硝酸鹽氮及硝酸鹽氮之和.分析圖 6(a)可知, R1中總氮平均損失為24.94%, 且在厭氧階段, R1和R2中COD急劇減少, 同時亞硝酸鹽氮和硝酸鹽氮都減少, 可能是由于厭氧階段反應器中發生了短程反硝化和反硝化.厭氧結束后, R1中COD濃度降到29 mg·L-1, 由于在曝氣階段顆粒污泥會形成內部厭氧區, 故會發生同步硝化反硝化作用, 在周期末COD濃度降到21 mg·L-1.分析圖 6(b)可知, 基于同樣的原因, R2中平均總氮損失為33.55%.由于R2中平均顆粒粒徑較R1顆粒平均粒徑大, 具有很好的層理結構, 且在曝氣階段中溶解氧在顆粒內部的滲透深度一般為100~200 μm, 故顆粒粒徑越大內部的缺氧區越大, 因此R2中顆粒污泥系統具有更強的同步硝化反硝化作用.在厭氧結束后, R2中COD濃度降低到29 mg·L-1, 在周期末, R2中COD濃度為10 mg·L-1較R1出水低.說明R2顆粒污泥系統較R1系統對進水中COD有更好的去除.
(1) 在普通活性污泥中分別接種好氧顆粒和除磷顆粒歷經42 d和56 d均實現了亞硝化污泥顆粒化, 且能縮短顆粒化時間, 好氧顆粒誘導絮狀污泥顆粒化優于除磷顆粒.具體聯系http://www.dowater.com更多相關技術文檔。
(2) 在COD負荷、氨氮負荷分別由0.2 kg·(m3·d)-1增加為0.5 kg·(m3·d)-1和0.4 kg·(m3·d)-1增加為0.5 kg·(m3·d)-1時, 添加除磷顆粒的污泥系統會使污泥系統發生膨脹, 導致系統長期運行失敗, 不適用于C/N比較高的進水水質; 添加好氧顆粒的污泥系統能適應水質變化, 耐沖擊負荷, 能長期穩定運行.